本治験は目標登録症例数を達成し被験者の募集を終了いたしました
関係機関ならびにご参加いただいた全国19の実施医療機関、被験者の患者様やご家族のご協力の下、円滑に症例登録を達成することができました。
今後、集積された治験データの解析を行い、薬事承認申請などのプロセスを進めて参ります。
早期アルツハイマー病患者を対象とした検証的試験概要
治験課題名
早期アルツハイマー病患者を対象としたLIPUS-Brain経頭蓋低出力パルス波超音波治療装置の有効性及び安全性を評価するための検証的試験

治験の目的
今回の治験では、軽度アルツハイマー病および軽度認知障害の患者さんを対象として治験機器による超音波治療を行い、その有効性と安全性を調べることを目的としています
医療機器の開発の一般的な進め方
-
- 基礎研究
-
- 非臨床試験(動物試験)
- 動物などを用いて試作機器の性能や安全性等を調べます。
治験
-
- 探査的試験
- 実際に少人数の患者さんを対象として有効性と安全性、適切な使用方法を確認します。
-
- 検証的試験
- より多くの患者さんを対象として有効性と安全性を検証します。
※本試験はこの最終段階にあたります。
-
- 厚生労働省へ申請
-
- 審議・承認
-
- 販売
治験情報サイト
下記公開サイトで治験情報がご確認頂けます。
1.臨床研究等提出・公開システム
臨床研究実施計画番号:jRCT2032230125
2.臨床試験登録サイト「ClinicalTrials.gov」(A Pivotal Study of LIPUS-Brain in Patients With Early Alzheimer’s Disease – Full Text View – ClinicalTrials.gov)
登録番号:NCT05983575
治験への参加方法
治験への参加にあたっては、患者様ご自身で治験を実施する医療機関を受診していただき、患者様が治験基準に適合するかを医師が判断する必要があります。
弊社が治験参加のお申込みをうけたまわることや、弊社から医療機関をご紹介することはできませんので、ご理解賜りますようお願い申し上げます。
治験への参加基準
治験に参加するには、医師によって参加基準を満たしているか評価を行います。
以下の項目は参加基準の一部となります。
同意していただいた後でも、検査の結果などによっては参加いただけない場合もありますのでご了承ください。
1.以下の項目に当てはまる方
- ① 患者さんご本人とその代諾者の双方から、文書による治験参加の同意が得られている方
- ② 50歳以上90歳未満の方
- ③ 治験期間中、以下の(ア)~(エ)の条件をすべて満たすパートナー/情報提供者がいらっしゃる方
- (ア) 患者さんご本人と同居あるいは連絡を行っていること
- (イ) 患者さんご本人の日常生活動作および体調の観察ができること
- (ウ) 本治験で決められた検査や試験に常に立ち会うことができること (エ) 薬の服用の管理ができると医師より判断されること
- ④ 同意いただく前の約1年(48週間)以内あるいはスクリーニング時の検査で軽度アルツハイマー病または軽度認知障害であると診断された方
2.以下の項目に一つでも当てはまる方は、本治験には参加いただけません。
- ①登録時から前12週間以内に、なんらかの症状がともなう脳梗塞または脳出血を起こしている方
- ②登録時に、悪性腫瘍(がん)を患わずらっている方、あるいは登録時から5年以内に悪性腫瘍(がん)の治療を受けていた方(切除治癒した上皮内癌を除く)
- ③登録時にてんかんである、もしくは過去にその状態であった方
- ④頭蓋内に人工物が埋め込まれている方
- ⑤脳外科手術(血管内治療を含む)をしたことのある方
- ⑥登録時に、妊娠中または妊娠を希望している方
- ⑦他の臨床研究や治験に参加している方

治験の方法
今回の治験では、各検査の結果から参加いただけるかどうかを確認した後に治験機器による超音波治療を開始します。ここで実治療群(実際に超音波治療を受ける)とプラセボ治療群(超音波が出ないように設定した装置を用いるので、超音波治療を受けない)のいずれかに、無作為に割り当てられます。
この治験は合計220名(プラセボ治療群110名、実治療群110名)の患者さんに参加していただく予定です。どちらの群になるかは、担当医師にも患者さんにもわかりませんし、選ぶことができません。
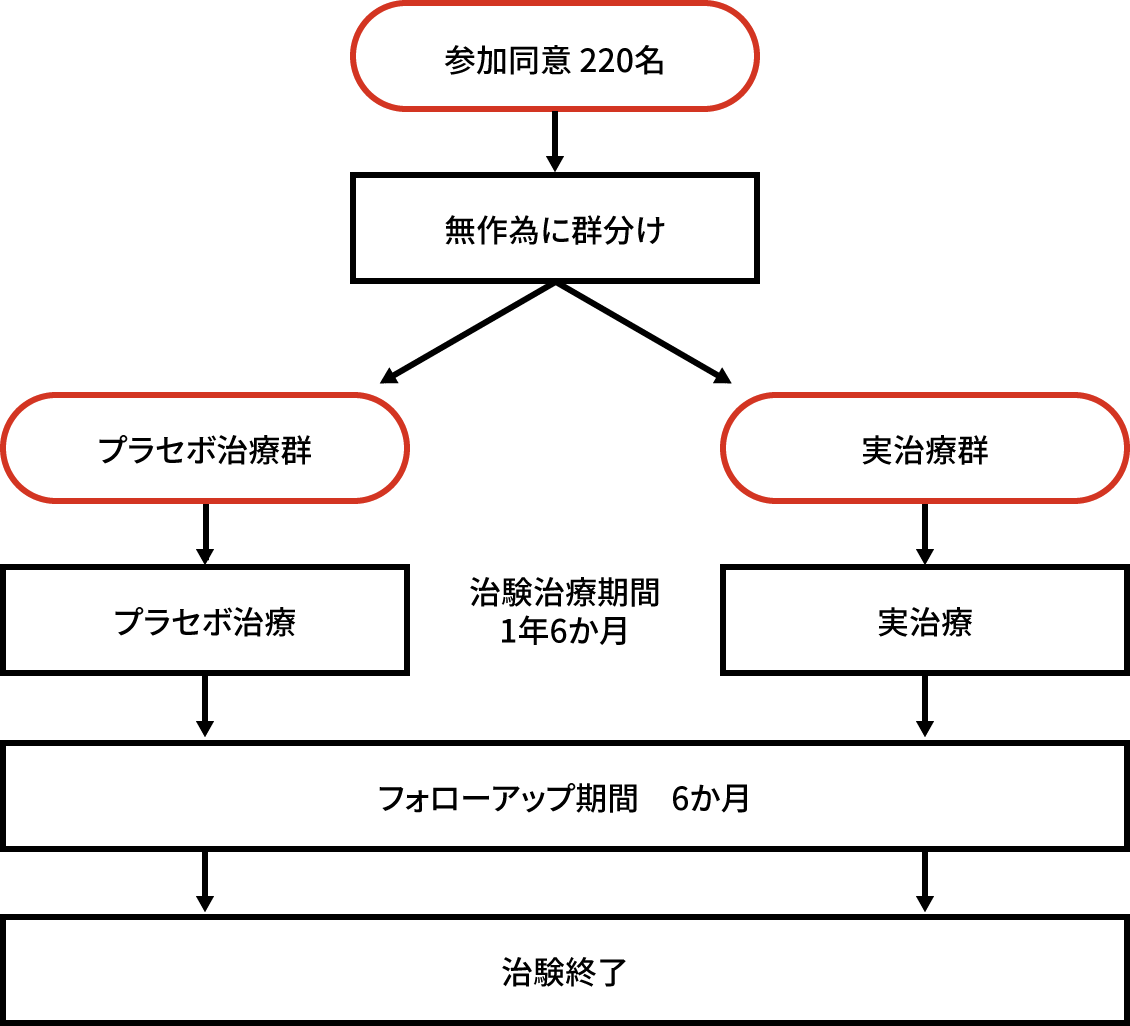
治験のスケジュール
治験治療は、頭にヘアバンドのようなもので両方のこめかみに近い部分に固定した治験機器から超音波を出すことにより行います。痛みはないので麻酔はしません。必要なときは、治療の途中でトイレに行くこともできます。
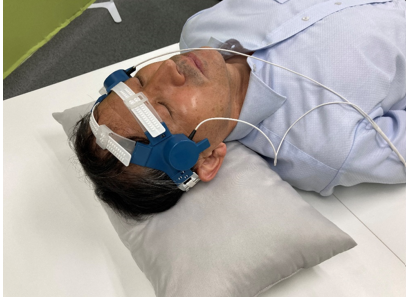
イメージ写真
治験治療は、1回20分です。間に5分間の休憩を入れて、1日に3回実施します。これを1セットとしています。1セットあたり約1時間かかることになります。治療をする6日間は、1日おきに来院していただき合計3セット治験治療を実施し、これを1クールとします。12週間ごとに1クールの治験治療を計6回(0、12、24、36、48、60週目)行います。
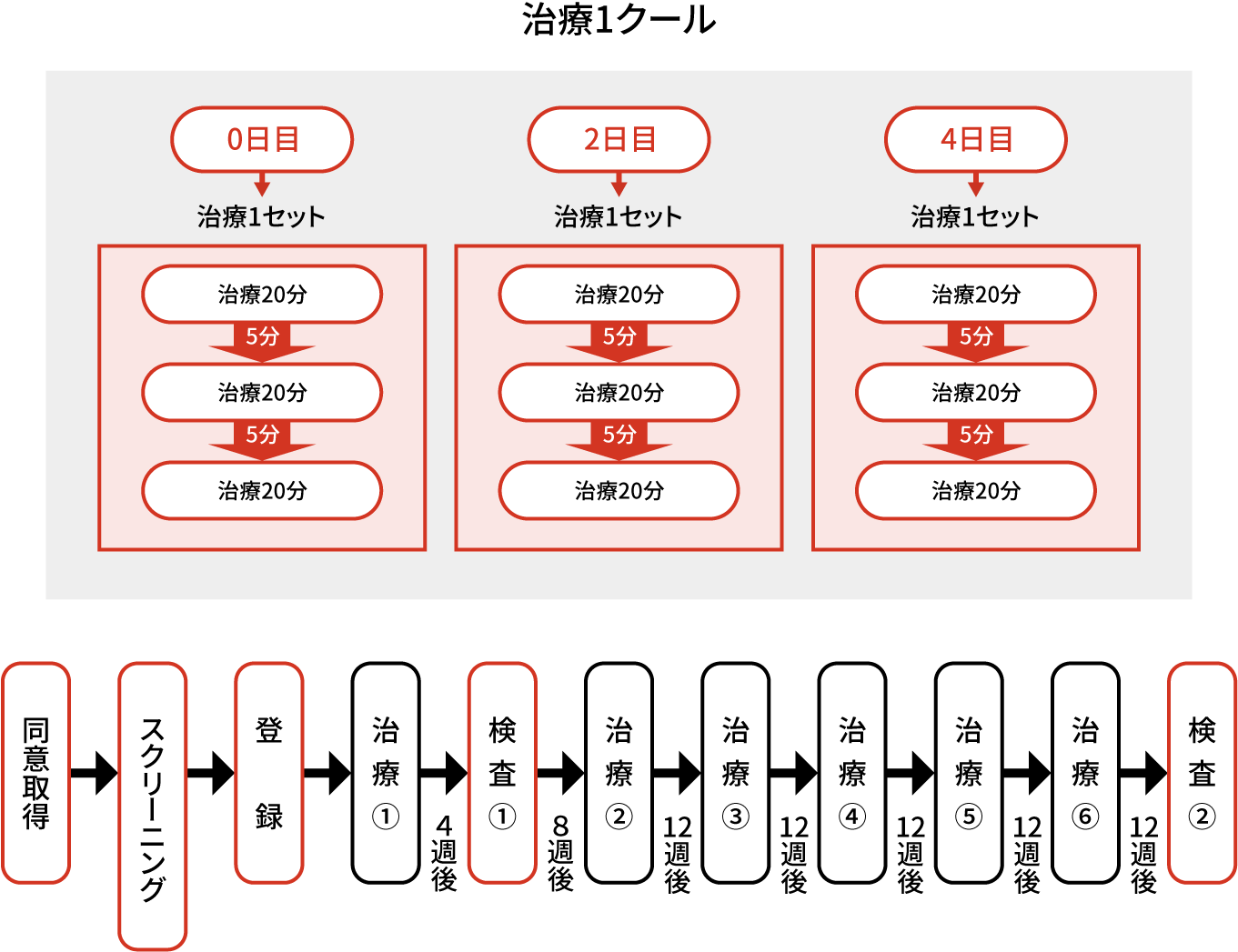
治験期間
治験期間は2023年8月~2026年10月を予定しております。
【治験に関する問い合わせはこちら】
※お電話でのお問い合わせはご遠慮ください
治験ニュース
透明性ガイドライン
弊社は、国民の生命・健康に関わる生命関連企業として、一般社団法人日本臨床検査薬協会の「企業活動と医療機関等の透明性ガイドライン」及び日本医療機器産業連合会の「医療機器業界における医療機関との透明性ガイドライン」の趣旨に賛同し、弊社が行うあらゆる活動の透明性をこれまで以上に高め、社会からのさらなる高い信頼を得られることを目指し、ここに「医療機関等との関係の透明性に関する指針」を定め、弊社における行動指針といたします。
透明性ガイドライン
【透明性ガイドラインによる支払い情報の開示】
弊社は、一般社団法人日本臨床検査薬協会の「企業活動と医療機関等の透明性ガイドライン」及び日本医療機器産業連合会の「医療機器業界における医療機関との透明性ガイドライン」に従い、この情報を公開しております。
公開情報をご覧いただく際は、以下の条件にご同意、ご確認の上でご利用ください。
公開情報は、弊社内処理において精意正確性を期して作成されたデータですが、完全な正確性を保証するものではなく、事後修正される場合があります。
情報アクセス・利用によって財産上、精神上の損害が発生しても、弊社は一切その責任を負いかねます。
情報アクセス・利用において、不法あるいは不正な目的をもって行うものではないこと。
公開情報に関するお問合せについては、一切応じられません。
金額は、円単位です。
